
早在2025年6月,专注于失明疾病基因疗法的开创性生物技术企业Ocugen透露已与韩国一家领军制药与医疗保健企业签署了一份具约束力的条款清单。9月15日,这个“神秘”合作对象的谜底终于揭晓。
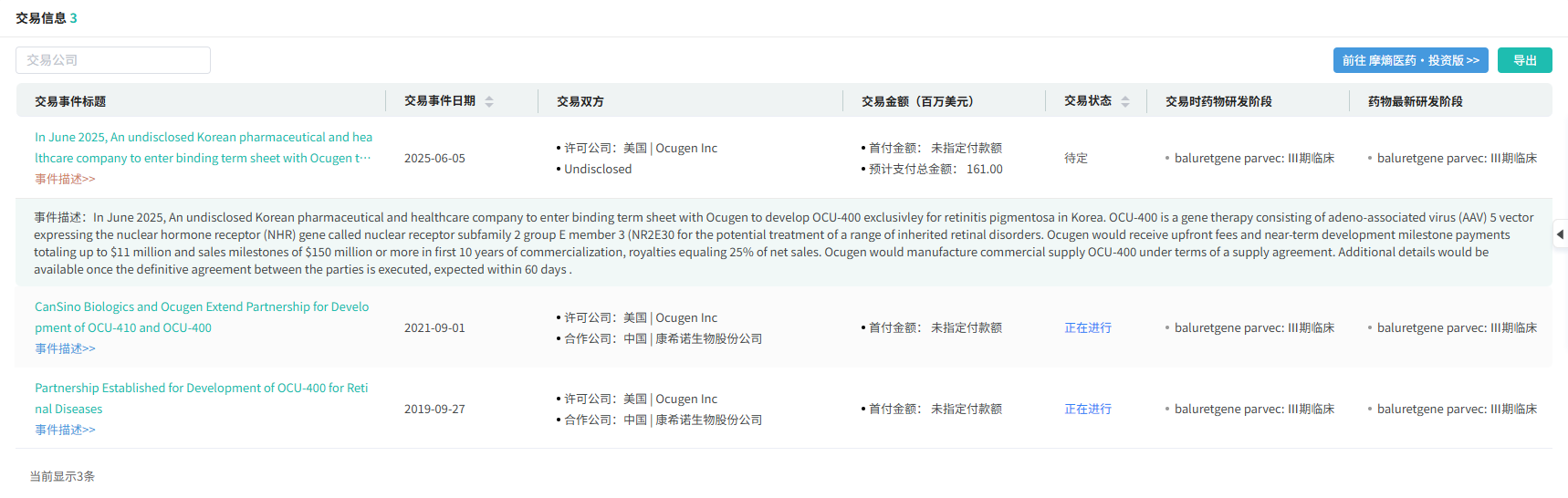
截图来源:摩熵医药数据库
2025年9月15日,Ocugen宣布与韩国领先制药企业Kwangdong Pharmaceutical签署许可协议,授予后者针对视网膜色素变性(RP)的新型修饰基因疗法 OCU400 在韩国的独家权益。
根据该许可协议,Ocugen 将获得总计最高750万美元的首付款及近期开发里程碑付款;在韩国每实现1,500万美元销售额时,公司还将获得150万美元的销售里程碑,商业化前10年的潜在销售里程碑为1.8亿美元或更多。此外,Ocugen将对 Kwangdong产生的 OCU400 净销售额收取25%的特许权使用费。Ocugen将依据供应协议负责 OCU400的商业化生产供应。

受此消息影响,公司股价上涨12%。
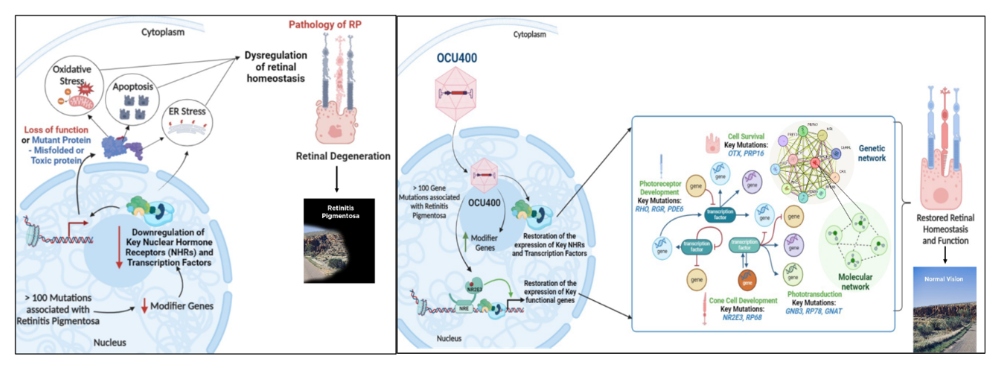
OCU400 是Ocugen用于治疗视网膜色素变性(RP)的创新疗法。OCU400 是基于核激素受体 (NHR) 基因NR2E3的基因修饰治疗产品。该基因调节视网膜内的多种生理功能,例如光感受器发育和维持、代谢、光传导、炎症和细胞存活。RP 患者的视网膜细胞具有功能失调的基因网络,而 OCU400可重置该网络以重建健康的细胞稳态,这有可能改善 RP 患者的视力。
Ocugen公司于2025年1月13日宣布了其1/2期针对 OCU400 临床试验为期两年的安全性和有效性更新结果。研究显示与未接受治疗的对侧眼睛相比,接受OCU400治疗的眼睛的低亮度视力 (LLVA) 显著提高了2行(ETDRS图表上的10个字母)。这种治疗效果在所有受试者中均具有统计学意义(p=0.01)。
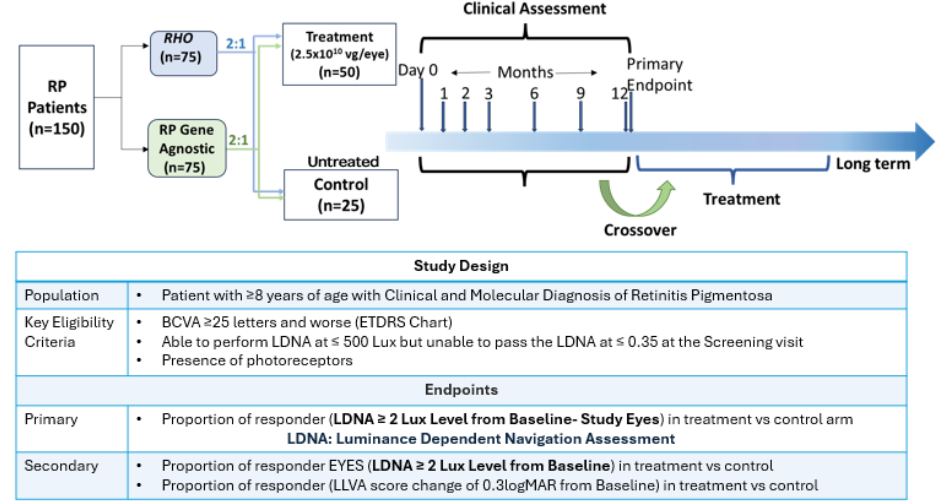
Ocugen目前正在推进 OCU400 的III期临床开发,3期liMeliGhT试验的给药正在进行中,计划于2026年向美国 FDA 递交生物制品许可申请(BLA)。Kwangdong拟采用 Ocugen的临床数据及 BLA 申报资料,作为其在韩国获批监管上市的重要组成。
Ocugen在新闻稿中表示,韩国约有7,000名视网膜色素变性(RP)患者,占美国市场规模的约7%。OCU400为Kwangdong提供了帮助数千名面临视力丧失患者的机会。一旦 OCU400 在韩国获得监管批准,Kwangdong将成为韩国眼科基因疗法领域的领军者。
Kwangdong是韩国排名前五的制药与保健企业,产品组合涵盖处方药及非处方保健品,并持续投入研发创新,重点布局后期、高影响力的颠覆性技术。
Kwangdong 董事长兼首席执行官 SungWon Choi 表示:“我们非常高兴能为韩国 RP 患者及治疗他们的医疗专业人士提供全新的治疗选择。对 Kwangdong 而言,与Ocugen的合作意义非凡,它将与我们现有的老花眼及儿童近视管线一起,进一步强化公司在眼科领域的布局。待OCU400正在进行的临床试验完成后,Kwangdong 将全力以赴,尽快把这一产品引入韩国市场。”
参考资料:公司公告
想要解锁更多药企信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发情况、年度报告、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!














































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论