
9月15日,药物临床试验登记与信息公示平台官网显示,澳宗生物登记了一项评价 TTYP01片(依达拉奉片)治疗早期症状性阿尔茨海默病(AD)的有效性和安全性的前瞻性、国际多中心、随机、双盲、平行、安慰剂对照的 II 期临床研究。
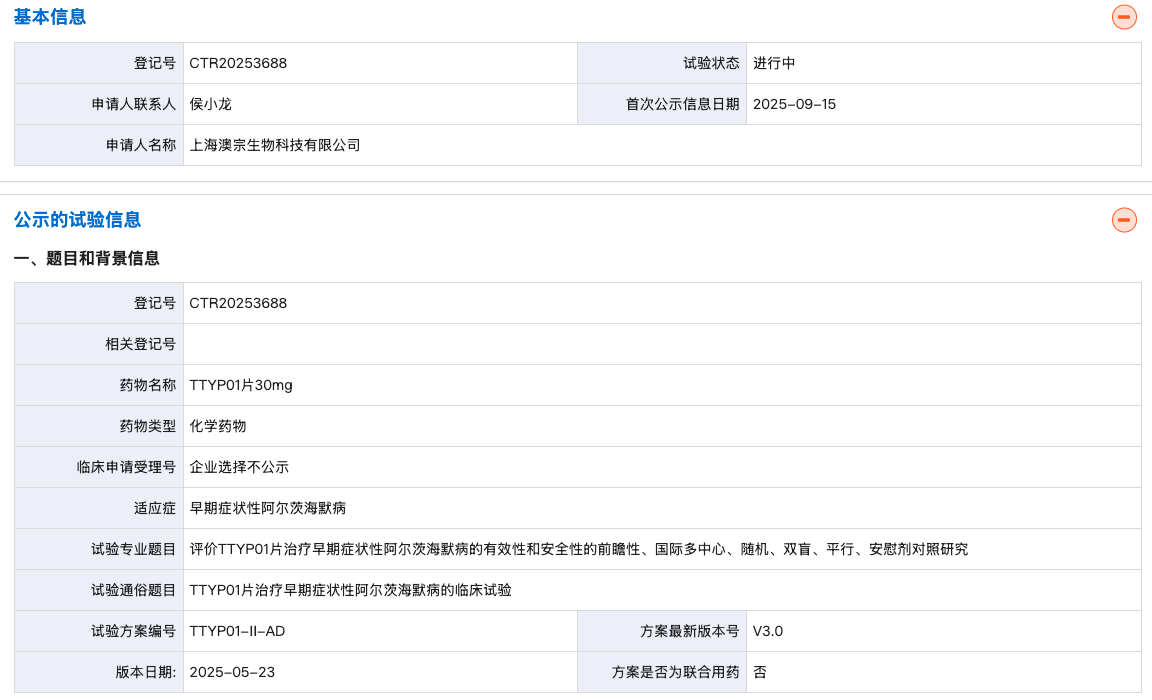
该研究旨在评估 TTYP01片治疗早期症状性 AD 的疗效、安全性和耐受性。受试者随机分组,接受 TTYP01 片 30mg 和安慰剂片 30 mg 治疗,用药时程为核心期 78 周,进入扩展阶段参与者累计104 周。
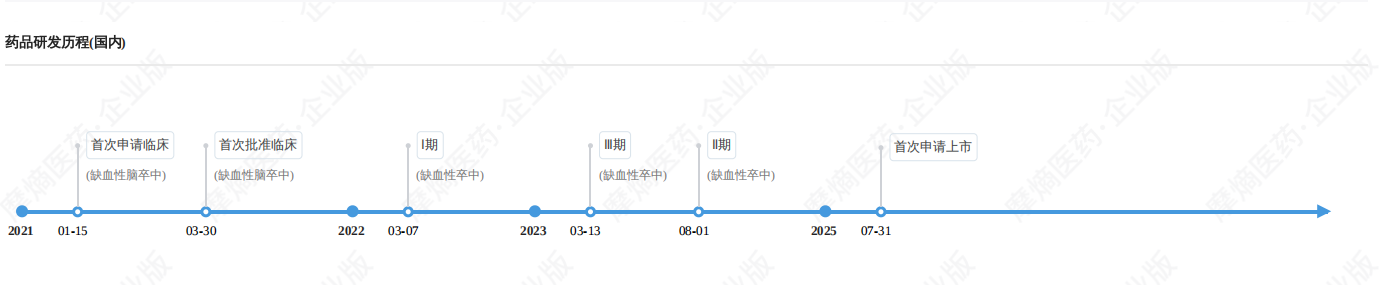
7月31日,华东医药全资子公司杭州中美华东制药有限公司申报的依达拉奉片上市许可申请正式获得受理,申报适应症聚焦于改善急性缺血性脑卒中(Acute Ischemic Stroke, AIS)所致的神经症状、功能障碍,并提升患者日常生活能力。














































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论