
近期金斯瑞生物科技表示:根据此前公告,内容有关南京蓬勃和礼新医药订立的经重述及经修订许可协议,根据该协议,南京蓬勃同意授予礼新(其中包括)一项独家全球可转让许可(包含分许可权),许可专利披露抗PD-1单域抗体和相关专有技术,由此礼新可针对许可专利进行开发、生产、商业化及以其他方式应用许可产品,以用于全球所有用途。
截至2025年6月27日,南京蓬勃及镇江蓬勃生物科技有限公司(公司非全资附属公司,与南京蓬勃统称“蓬勃”)已收到经重述及经修订许可协议项下约2.138亿美元(扣除代扣代缴所得税后)的付款。
该等付款由下列各项组成:(i)首付款;(ii)达成首个里程碑获得的里程碑付款;(iii)与经重述及经修订许可协议项下经许可的抗PD-1单域抗体有关的分许可收入。
抗PD-1单域抗体被用于礼新医药开发的在研PD1/VEGF双特异性抗体LM-299,该双特异性抗体LM-299已获得新药临床研究批准。该等款项的到账将进一步充盈蓬勃的现金储备并增强其核心竞争力。
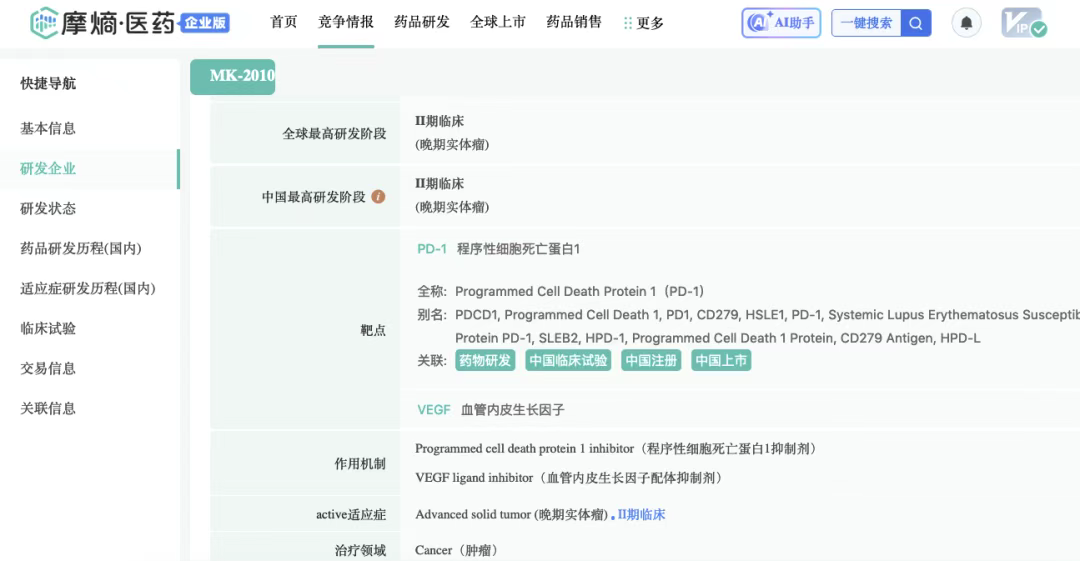
截图来源:摩熵医药数据
此前在2024年11月14日,美国制药巨头默沙东(MSD)宣布,已与中国礼新医药正式签署了一项规模最多高达32.88亿美元的战略合作协议。根据协议条款,默沙东将独家获得礼新医药正在研发的创新PD-1/VEGF双特异性抗体LM-299(默沙东研发代码MK-2010)的全球开发权、生产权及商业化许可。税前首付款即达5.88亿美元。
根据与礼新医药最新修订并确认的协议条款,蓬勃生物在新药研究申请(IND)获批至许可产品一期临床试验完成的阶段内,将享有两大核心财务权益:一是对于此期间发生的任何再许可活动,蓬勃生物有权获取40%的预付款及25%的其他里程碑款项;二是其还将从礼新公司所获得的特许使用费(即收入分成)中分得25%的比例。

截图来源:摩熵医药数据
另外,业界也比较关注礼新医药给投资人此次交易后分配多少,毕竟新药投资的周期太长,很多基金没有回报。
期待更多的中国交易产生,目前已经成为全球创新药的策源地。
参考:NMPA/CDE;
摩熵医药数据pharma.bcpmdata.com(原药融云数据);
FDA/EMA/PMDA;
公司官方;
https://data.eastmoney.com/notices/detail/01548/AN202506301700147299.html;
ProBio;
MSD;
https://pharma.bcpmdata.com/database/24/detail/441/5f78a0bc1a8ea0766da327f5dde906d2;等等。
想要解锁更多药企信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!














































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论