
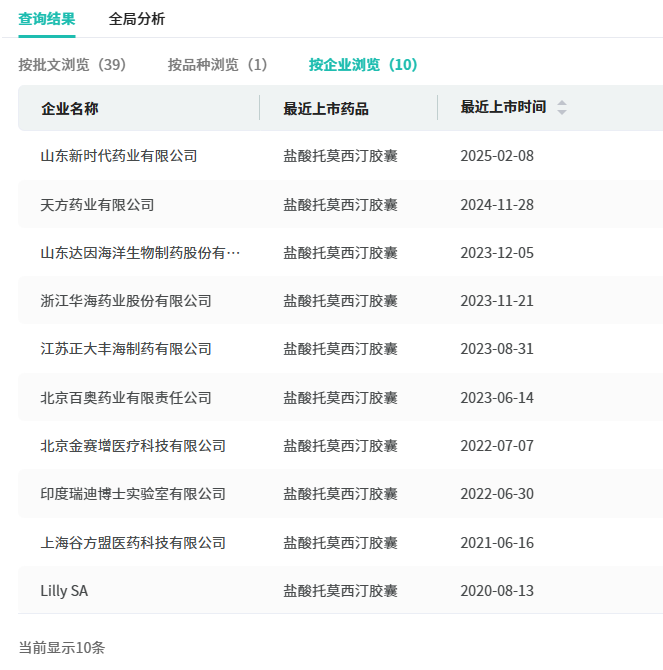
9月26日,据CDE官网显示,太极集团旗下西南药业提交的盐酸托莫西汀胶囊4类仿制上市申请已获受理,该产品原研于2024年1月停止中国市场供应。据摩熵医药数据库显示,目前盐酸托莫西汀在国内主要有胶囊剂和口服溶液,其中,持有胶囊剂生产批文的药企(进口+国产)达10家。
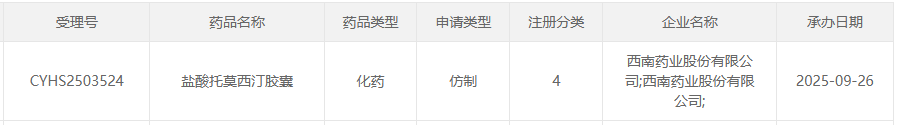
截图来源:CDE
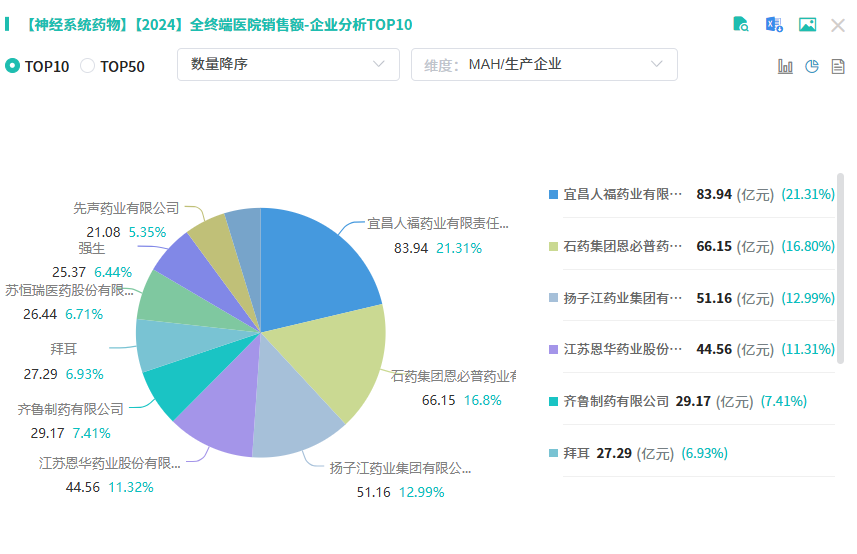
盐酸托莫西汀(择思达)原研为礼来,2002年在美国上市,主要用于治疗儿童和青少年的注意缺陷/多动障碍(ADHD)的非兴奋型药物,也是美国儿童青少年精神病协会(AACAP)推荐的治疗ADHD的一线药物。2007年,盐酸托莫西汀胶囊在中国获批上市,与再普乐、百优解及欣百达并称为礼来在中国中枢神经产品线中的四大核心药品。摩熵医药数据显示,盐酸托莫西汀胶囊在2021年全终端医院市场的销售额突破3亿元,同比增长率达46.64%,2025年(截至Q2)其销售额已超1亿元。















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论