
9月15日,石药集团发布公告,其自主研发的ALMB - 0166获国家药监局批准,将在中国开展Ⅱ期临床试验,以评估其对帕金森氏症疗效。近期,石药集团新药研发捷报频传,其中SYH2066(化药1类)在中国获批临床,SYS6036注射液、度普利尤单抗注射液相继获批临床试验。此外,KN026(安尼妥单抗注射液)新药和司美格鲁肽注射液上市申请也已获受理。

截图来源:石药集团企业公告
ALMB - 0166是一款同类首创(First-in-class)的创新药物,它精准靶向全新作用点——半通道膜蛋白Connexin 43(Cx43),属于人源化单克隆抗体抑制剂,由石药集团旗下附属公司AlaMab Therapeutics Inc.自主研发而成,专门用于治疗帕金森氏症、急性缺血性脑卒中、急性脊髓损伤等神经系统疑难病症。
帕金森氏症作为全球范围内第二大高发的神经退行性疾病,其核心病理特征为黑质多巴胺神经元逐步退变以及路易小体的异常形成。据摩熵医药数据库统计,2024年全终端医院神经系统药物销售额超1000亿元,而2025年(截至Q2)销售额已超500亿元,市场潜力巨大。此次,石药集团的ALMB - 0166成功获国家药监局批准开展Ⅱ期临床试验,为千亿市场注入强劲动力。
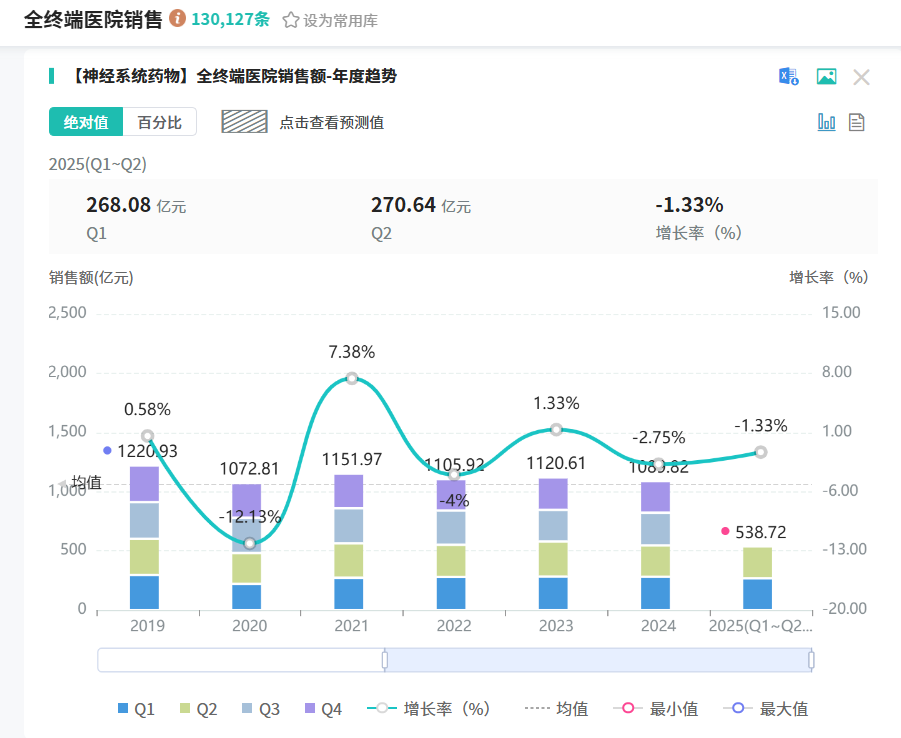
截图来源:摩熵医药全终端医院销售数据库
作为传统医药巨头,石药集团在坚持传统的仿制药和改良药研发的同时,也在加速转向创新药研发,并进入收获期。近期,先是SYH2066(化药1类)、SYS6036注射液、度普利尤单抗注射液相继获批临床,接着,KN026(安尼妥单抗注射液)新药和司美格鲁肽注射液上市申请获受理,而且KN026近期还将提交二线胃癌适应症上市申请。
在ADC药物领域,石药集团成绩斐然。目前已有11款ADC药物进入临床阶段,其中EGFR ADC药物SYS6010已启动EGFR突变非小细胞肺癌二线治疗的Ⅲ期临床试验,预计2026年提交上市申请,有望为肿瘤患者带来新的治疗选择。
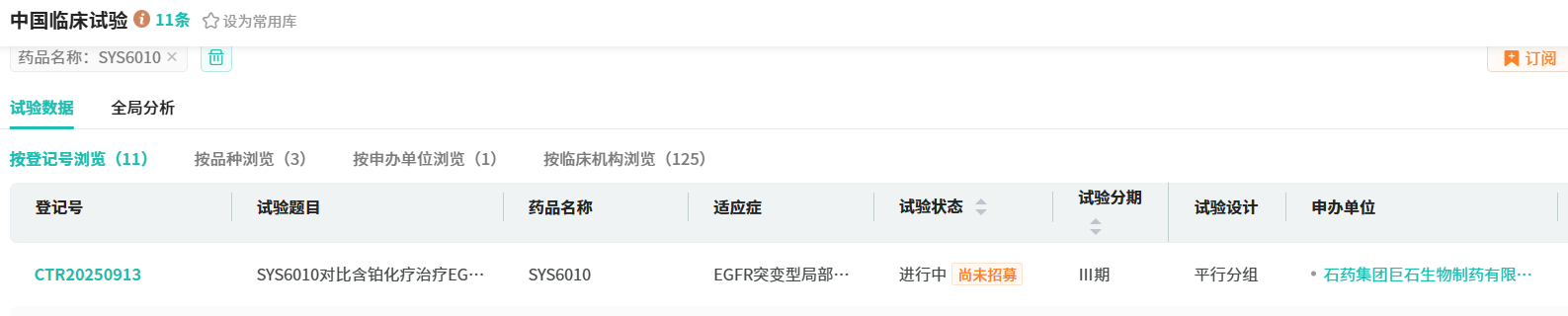
截图来源:摩熵医药中国临床试验数据库
石药集团(含子公司)在创新研发领域成果丰硕。2025年至今,摩熵医药数据库统计显示,共有SYHA-1813口服溶液、SYH-2067胶囊、SYH-2051片、SYH-2066片等12款1类新药获批临床,涉及系统用抗感染药物、心血管系统药物、消化系统与代谢药物、抗肿瘤药物和免疫机能调节药物四大治疗领域。












































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论