
中国药品专利期限补偿制度(Patent Term Extension, PTE)落地成果揭晓—八款药品成功突围,涵盖单抗、融合蛋白、小分子及中成药四大品类(截止撰稿日2025.07.04)。
这些药物不仅代表着本土与跨国药企的研发突破(如荣昌生物泰它西普、罗氏阿替利珠单抗),更折射出PTE制度对新药(创新药/符合要求的改良新)市场独占期延展的核心价值。
本文通过剖析8款获PTE药物的专利(如佩索利单抗的IL-36R靶点全球首创新药地位)、上市后销售轨迹(如卡瑞利珠单抗三年稳守14亿市场),以期为后来者提供思考。
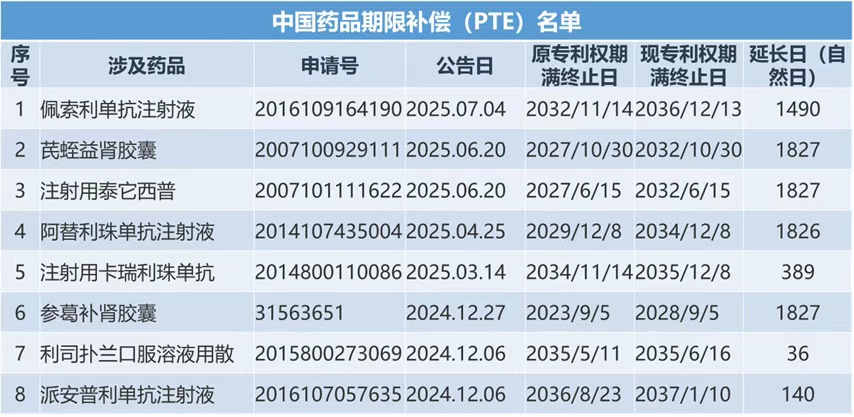
数据来源:中国知识产权局-中国专利公布公告,表格自制
1.1.1佩索利单抗注射液
圣利卓®(佩索利单抗注射液)是同类首个阻断白介素-36受体 (IL-36R)激活的单克隆抗体,可抑制IL-36的信号传导,也是国内首个获批专门用于治疗成人泛发性脓疱型银屑病(GPP)发作的治疗药物。GPP是一种罕见病,中国患者约2万人,发病率低(1.403/10万)。
中国注册情况:中国2022年12月13日首次批准上市(静脉注射剂型),用于治疗成人泛发性脓疱型银屑病(GPP)发作;2024年3月,皮下注射剂型获批,用于减少GPP发作,实现全病程管理。
市场表现:2023年产生销售额,近两年院内销售额分别为42、444万元,销售量分别是8瓶、336瓶。
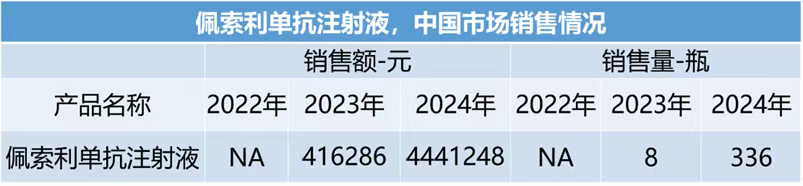
罕见病药物市场存在潜力,但需耐心和信心进行培育:佩索利单抗的销售数据(2023年仅8瓶,2024年336瓶)突显出罕见病药物上市初期的挑战:患者基数小、诊断率低(GPP易误诊为寻常银屑病)、市场教育成本比较高。然而,一旦建立信任(如通过临床证据和医生培训),需求可快速释放(2024年销售量激增);
专利策略是创新药商业化的核心驱动力:核心专利延长1490日直接延长了市场独占期,延长仿制药竞争。启示:药企应积极利用专利延长制度,并结合政策红利,最大化产品生命周期价值。
1.1.2芪蛭益肾胶囊
芪蛭益肾胶囊是第一个获批用于降低早期DKD患者尿白蛋白排泄率,延缓DKD的疾病进展,从而达到治疗DKD目的的中成药;弥补了目录内治疗早期DKD的中成药空白。
中国注册情况:中国2021年11月24日批准上市;
市场表现:2023年产生销售额,近两年院内销售额分别为0.17、0.68亿元,销售量分别是713、2892万粒。
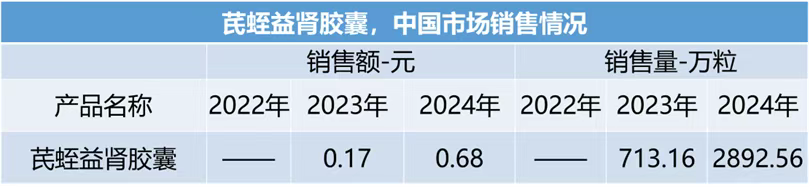
精准定位未满足需求,规避红海竞争:该产品聚焦早期DKD,与化药(如SGLT2抑制剂)形成协同而非替代,避免直接竞争。
中药创新药的政策红利与市场机遇:2024年销量激增,与医保支付加速医院准入强相关。启示:中药1类新药应优先布局医保谈判,利用政策支持快速覆盖基层市场。
1.1.3注射用泰它西普
泰它西普(Telitacicept,RC18,商品名:泰爱®)是荣昌生物自主研发的一款 BLyS/APRIL 双靶点融合蛋白创新药,可通过同时抑制 BLyS 和 APRIL 两个细胞因子的过度表达,「双管齐下」阻止 B 细胞的异常分化和成熟,从而治疗 B 细胞介导的多种免疫性疾病。
中国注册情况:中国2021年03月09日批准上市;
市场表现:院内市场,2022-2024年院内销售额分别为0.62、1.35和3.28亿元,销售量分别是7.62、16.46和41.05万支。
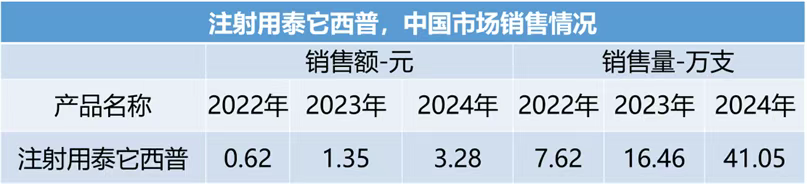
专利延长强化市场独占性:核心专利延长1827天(约5年),延长至2032年后(原专利2027年到期),延缓生物类似药竞争。
医保准入与商业化策略协同:2023年进入医保后,2024年销量激增149%(16.46万→41.05万支),体现“以价换量”成功。
1.1.4阿替利珠单抗注射液
阿替利珠单抗是罗氏研发的一种人源化单克隆抗体,作为程序性细胞死亡配体(PD-L1)阻断剂,2016年获得美国食品药品监督管理局FDA批准上市。阿替利珠单抗能与肿瘤细胞上的PD-L1结合,并阻断其与T细胞及抗原递呈细胞PD-1的相互作用,从而解除PD-1介导的免疫抑制,促进T细胞攻击肿瘤细胞。
中国注册情况:中国2020年02月11日批准上市;
市场表现:2022-2024年院内销售额分别为2.28、3.92、4.82亿元,销售量分别是0.70、1.20和1.47万支。
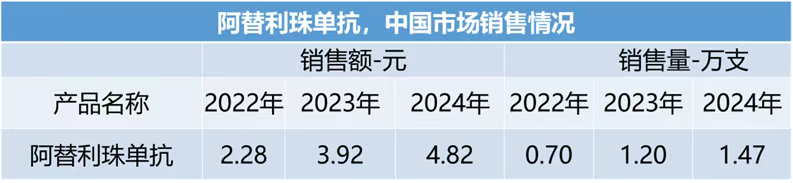
专利延长与生命周期管理:核心专利延长1826天(约5年),保护期延至2034年后,规避生物类似药冲击。
作为PD-L1(非PD-1)抑制剂,通过差异化机制避免红海竞争,维持溢价能力。
1.1.5注射用卡瑞利珠单抗
注射用卡瑞利珠单抗是一种人源化抗 PD-1 单克隆抗体,是肿瘤领域的重磅药物,于2019年5月获批上市,目前已在国内获批10项适应证,涉及鼻咽癌、肺癌、淋巴瘤、肝癌、宫颈癌等。
中国注册情况:中国2019年05月29日批准上市;
市场表现:2022-2024年院内销售额分别为14、14.23、14.62亿元,销售量分别是47.72、52.56和54.72万支。
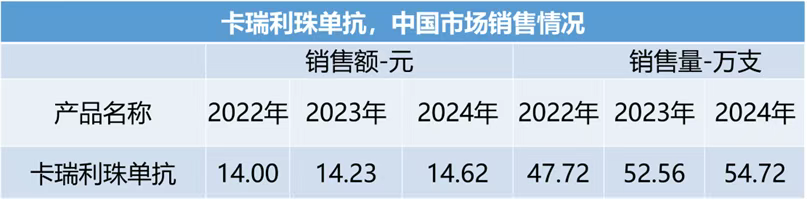
适应症广度优势未能明显转化为销售额增长:销售量增长14.7%(2022→2024),但单价下降9%,销售额几乎停滞,一定程度上反映中国PD-1市场内卷加剧,卡瑞利珠需通过“以价换量”维持份额。
1.1.6参葛补肾胶囊
参葛补肾胶囊是一种中药复方制剂,该药是新疆首个国家一类中药创新药(1.1类),也是全球首个以有效部位群复方配伍治疗抑郁症的中成药。其研发依托新疆天然药材资源(如太子参、淫羊藿),并纳入国家“重大新药创制”科技专项。
中国注册情况:中国2022年12月29日批准上市;
市场表现:2024年院内销售额及销售量分别为600万元,129.67万粒。
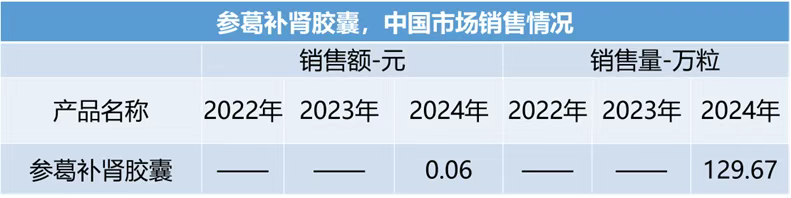
专利延长≠商业成功:参考泰它西普,参葛补肾胶囊需配套市场准入+剂型迭代+患者服务组合拳(参考泰它西普专利延长5年+剂型升级策略)。
避免“小众证型陷阱”:中医证型定位需兼顾患者基数与西医病种对接(如参考芪蛭益肾胶囊锚定DKD西医诊断标准)。
1.1.7利司扑兰口服溶液用散
利司扑兰是全球首个获批的直接以RNA为靶点发挥作用的小分子药物,可穿透血脑屏障,分布于中枢和外周,可提高全身多系统SMN蛋白水平,且保持稳定。利司扑兰用于治疗2月龄及以上的SMA(脊髓性肌萎缩)患者。
中国注册情况:中国2021年06月16日批准上市;
市场表现:2022-2024年院内销售额分别为0.03、0.33、0.56亿元,销售量分别是0.01、0.87和1.49万支。
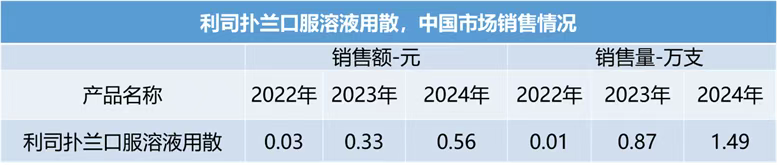
口服剂型颠覆治疗范式:口服剂型是罕见病药物破局关键(VS竞品诺西那生钠注射剂型),尤其适用于需终身治疗的神经退行性疾病。
专利36天延长难抵竞争冲击:专利生命周期管理需前置,36天延长暴露专利布局薄弱,建议绑定孤儿药资格申请延长(参考泰它西普1827天延长)。
1.1.8派安普利单抗注射液
派安普利单抗是全球首个采用IgG1亚型并进行Fc段改造的PD-1单抗。该产品是由康方生物自主研发、并由康方生物与中国生物旗下正大天晴药业集团合资的正大天晴康方负责后续开发和商业化。
中国注册情况:中国2021年08月03日批准上市;
市场表现:2022-2024年院内销售额分别为0.37、0.53、0.51亿元,销售量分别是0.78、1.42和1.35万支。
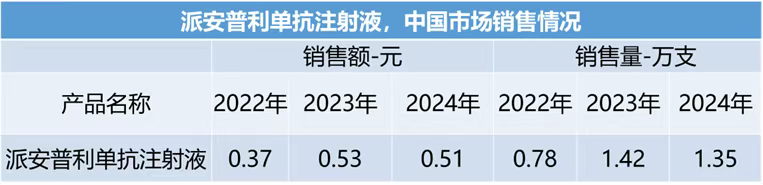
康方生物需重构支付体系,拥抱商保:2024年销量/销售额双降(销量-5%,销售额-4%),在PD-1内卷中陷入生存危机。并且2023年医保谈判出局(定价>0.4万/支 vs 行业均价0.27万),失去三甲医院准入资格。
肝癌适应症加速:派安普利单抗已在中国取得三项适应症批准,包括非小细胞肺癌、霍奇金淋巴瘤和鼻咽癌,同时也在推进肝癌、胃癌等适应症的临床研究。建议将HCC一线治疗Ⅲ期试验(NCT04892420)优先级提高,加快大癌症的布局。
总结
中国PTE制度已跨越政策适配期,步入企业专利战略能力的深水博弈阶段。首批八款药物的实践表明:单纯依赖专利延长期无法保障商业成功,建议构建全面的战略框架——以临床价值定义为根基(如利司扑兰以口服剂型突破血脑屏障,颠覆SMA注射治疗范式,解决居家给药痛点);以专利生命周期管理为骨架(如阿替利珠单抗获5年专利延长并同步开发皮下注射剂型,形成双重壁垒);以支付体系创新为血脉(如芪蛭益肾胶囊借PTE+医保实现基层放量年销0.17亿→0.68亿,开辟“西医病种+中医证型”新路径);以全球化布局为外延(参考阿替利珠欧美市场溢价)。
未来企业决胜关键在于PTE制度红利的转化:以专利延长期为轴心,剂型迭代与支付协同为双翼,铸造动态强化的市场护城河。企业需在产品仿制药大潮来临前,完成从政策响应者到专利战略家的蜕变。
参考资源:
注册:NMPA、CDE等官网
市场销售数据:IQVIA-CHPA数据库,院内销售数据
药品简介:各药品说明书及公开来源
专利数据:中国知识产权局-中国专利公布公告
作者简介:药丸,中国药科大学硕士毕业,具有法律及药学教育背景,拥有法律资格证和专利代理师资格证,致力研究药学和专利,做一颗有价值的药丸。
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!














































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论