
2020年前后,同种异体CAR-T(AlloCAR-T)疗法风头无两。作为传统自体CAR-T的升级方向,它承诺摆脱“一人一药”的定制化困境,实现“现货供应”,解决细胞治疗可及性的核心痛点。
资本市场对其青睐有加,Allogene Therapeutics等公司备受追捧。
然而,当AlloCAR-T仍在验证自身安全性与有效性的道路上稳步推进时,一场新的技术革命已然萌芽。
2025年3月,阿斯利康(AstraZeneca)以总价10亿美元收购了EsoBiotec,将其工程化纳米抗体慢病毒(ENaBL)平台及针对多发性骨髓瘤的BCMA CAR-T管线ESO-T01收入囊中。
6月,艾伯维(AbbVie)以高达21亿美元的全现金收购了专注于体内CAR-T的Capstan Therapeutics,获得了其靶向脂质纳米颗粒(tLNP)平台及在研管线CPTX2309(靶向CD19,用于自身免疫性疾病)。
巨头们的巨额押注,仿佛为In Vivo CAR-T加冕。这究竟是巨头的又一次华丽追逐,还是治疗革命的真正开端?
要点速览:
- Allo CAR-T临床领先但存在安全性挑战;In Vivo CAR-T起步晚,巨头押注其颠覆潜力。
- 两者商业化均面临瓶颈:Allo受制于生产复杂性与排斥风险,In Vivo需攻克递送效率与长期安全性。
表1 In Vivo与Allo CAR-T核心特点和临床进展
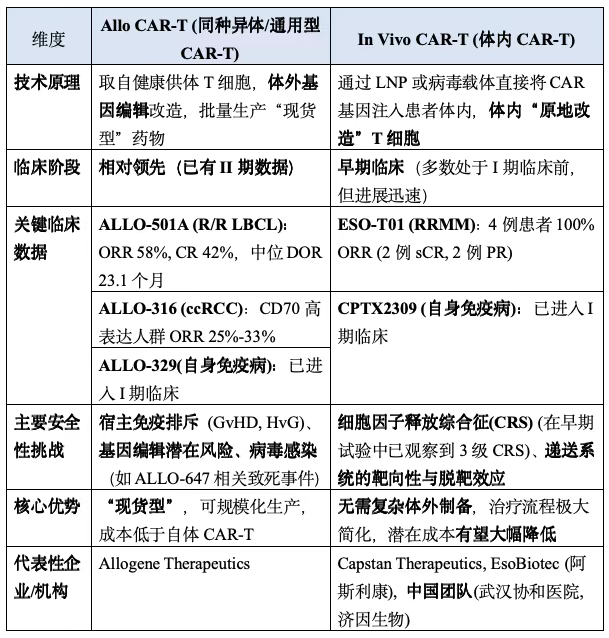
01看看谁快?临床进展的竞速赛
当前,Allo CAR-T的临床开发进度整体上领先于In Vivo CAR-T,已有较多的临床数据输出;而In Vivo CAR-T虽起步较晚,但发展迅猛,初步临床数据令人鼓舞。
1.1 Allo CAR-T:血液肿瘤数据积极,探索实体瘤
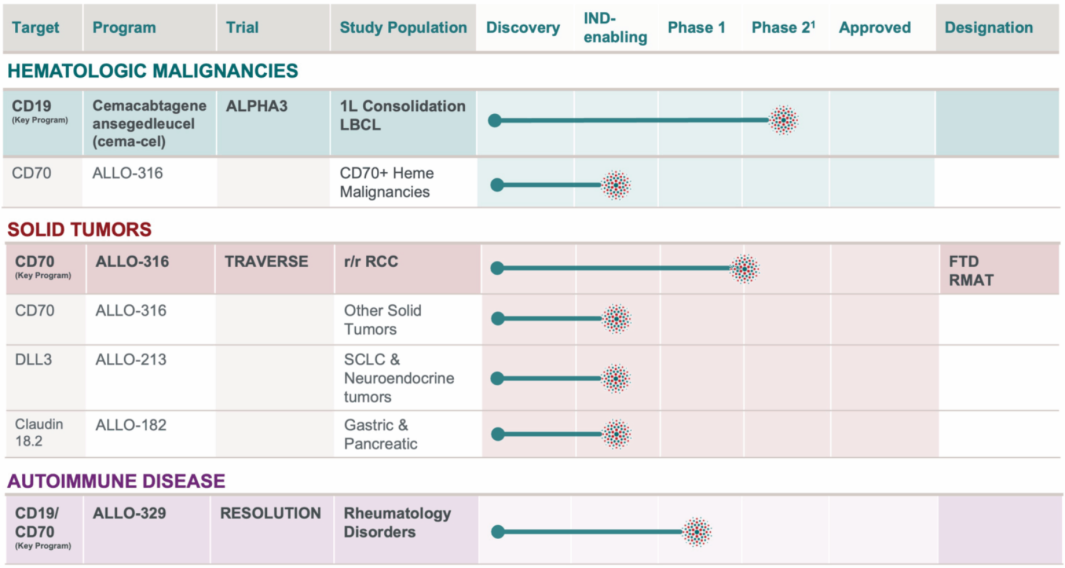
图1 AlloCAR T™ 产品管线针对多种肿瘤类型和自身免疫适应症
①肿瘤治疗方向进展迅速
在复发/难治性大B细胞淋巴瘤(R/R LBCL)中,Allogene公司的cama-cell(曾用名ALLO-501A,靶向CD19)显示了颇具前景的疗效。其Ⅰ期ALPHA2研究显示,经治患者中的客观缓解率(ORR)为58%,完全缓解率(CR)达42%。尤为重要的是,获得完全缓解的患者展现了持久的疗效,中位缓解持续时间(DOR)达到23.1个月。
表2 cama-cell治疗效果总结
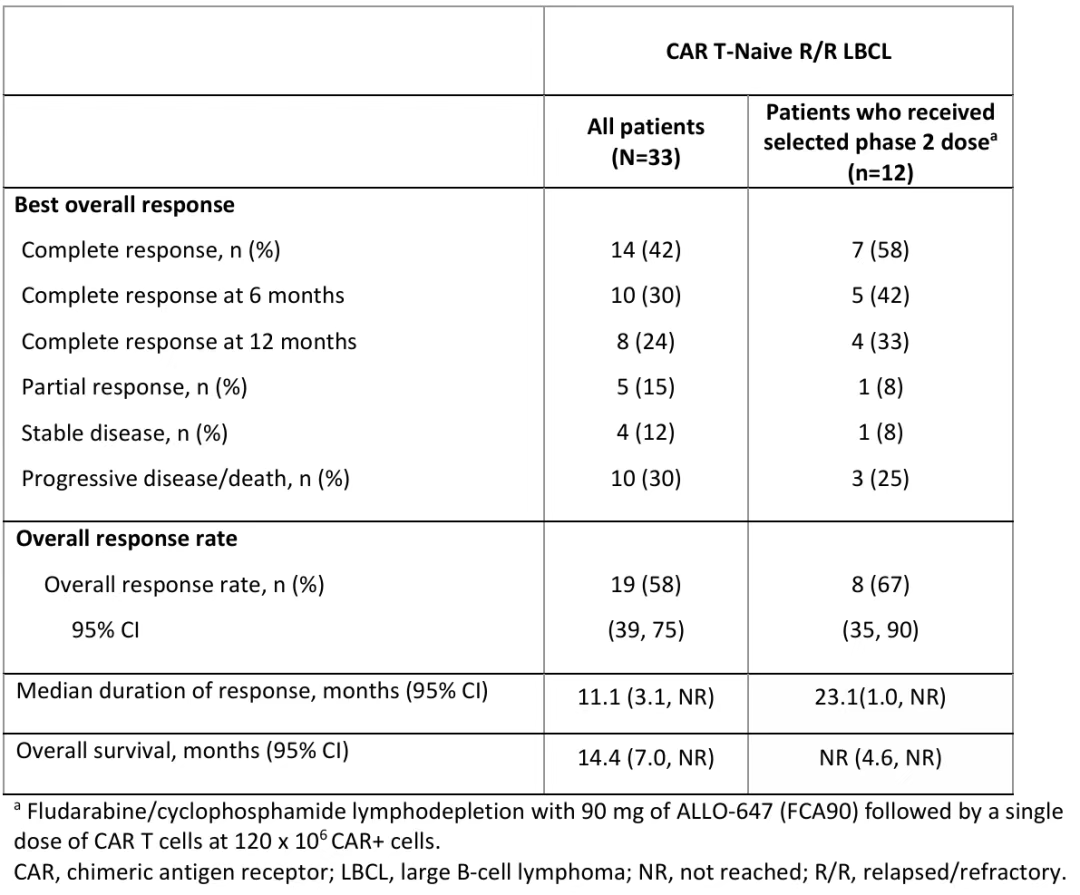
在挑战更大的实体瘤领域,Allo CAR-T也在积极探索。其靶向CD70的ALLO-316用于治疗晚期透明细胞肾细胞癌(ccRCC)的TRAVERSE研究显示,在CD70高表达(TPS≥50%)的患者中,确认的ORR为25%(其中1b期患者为33%)。
表3 ALLO-316治疗效果总结
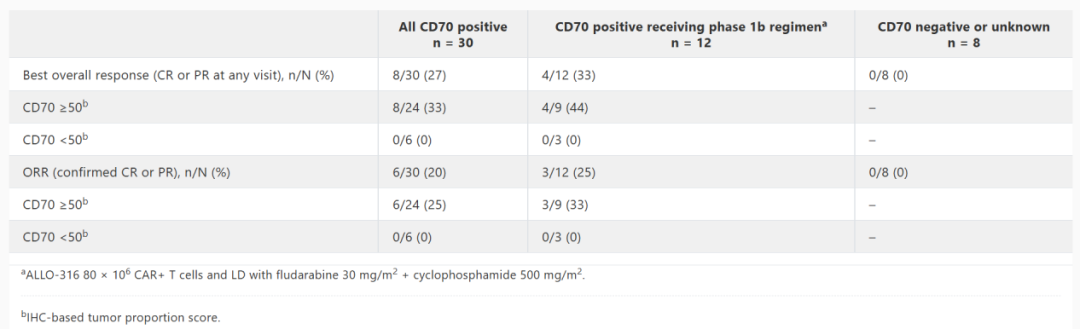
②自免拉开帷幕
4月,Allogene公司用于治疗自身免疫疾病的同种异体CAR-T疗法ALLO-329(靶向CD19、CD70)已进入I期临床阶段,并已获得美国FDA针对系统性红斑狼疮(SLE)、炎症性肌病(IIM)和系统性硬化症(SSc)的快速通道资格,计划在2025年底获得ALLO-329的初步概念验证(POC)数据。
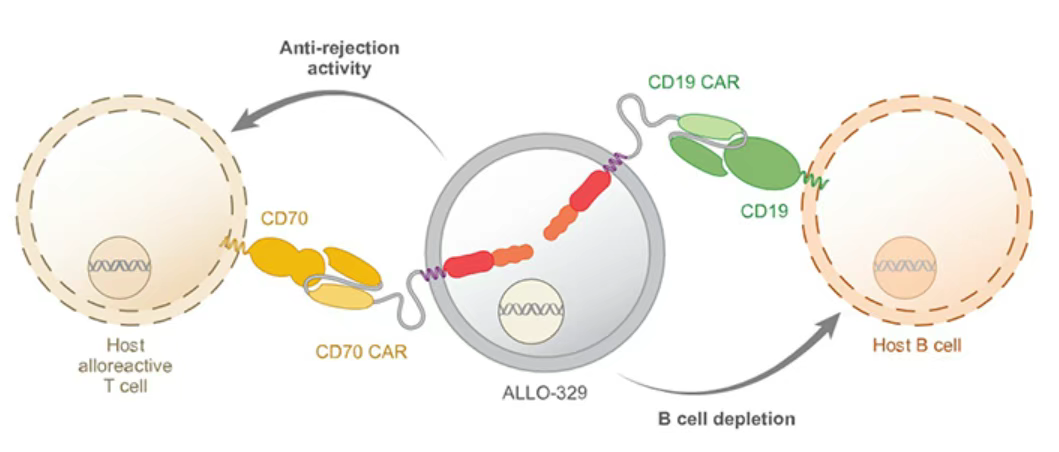
图2 ALLO-329作用机制
1.2 In Vivo CAR-T:初步人体数据验证可行性
尽管起步较晚,In Vivo CAR-T的临床进展令人瞩目,初步验证了其概念可行性。
①治疗血癌初见成效
EsoBiotec(现为阿斯利康子公司)的ESO-T01是第一个在人体临床试验中给药的体内BCMA CAR-T候选药物,由第三代免疫屏蔽细胞特异性慢病毒载体平台ENaBL开发,具有免疫屏蔽作用和抗吞噬作用。
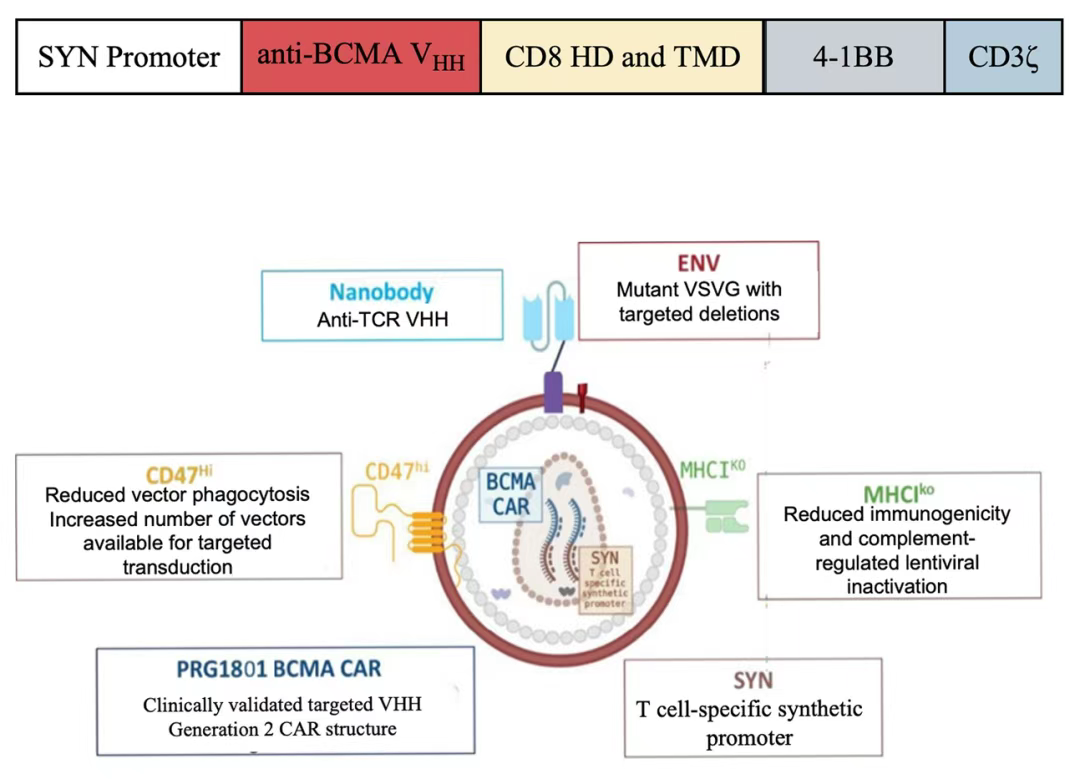
图3 ESO-T01的构造和设计机制
ESO-T01的一项首次人体(first-in-human)研究于今年7月发表于柳叶刀。4名复发/难治性多发性骨髓瘤患者接受单次输注后,实现了100%的客观缓解率(ORR),其中2例达到严格完全缓解(sCR),另外2例为部分缓解(PR)。
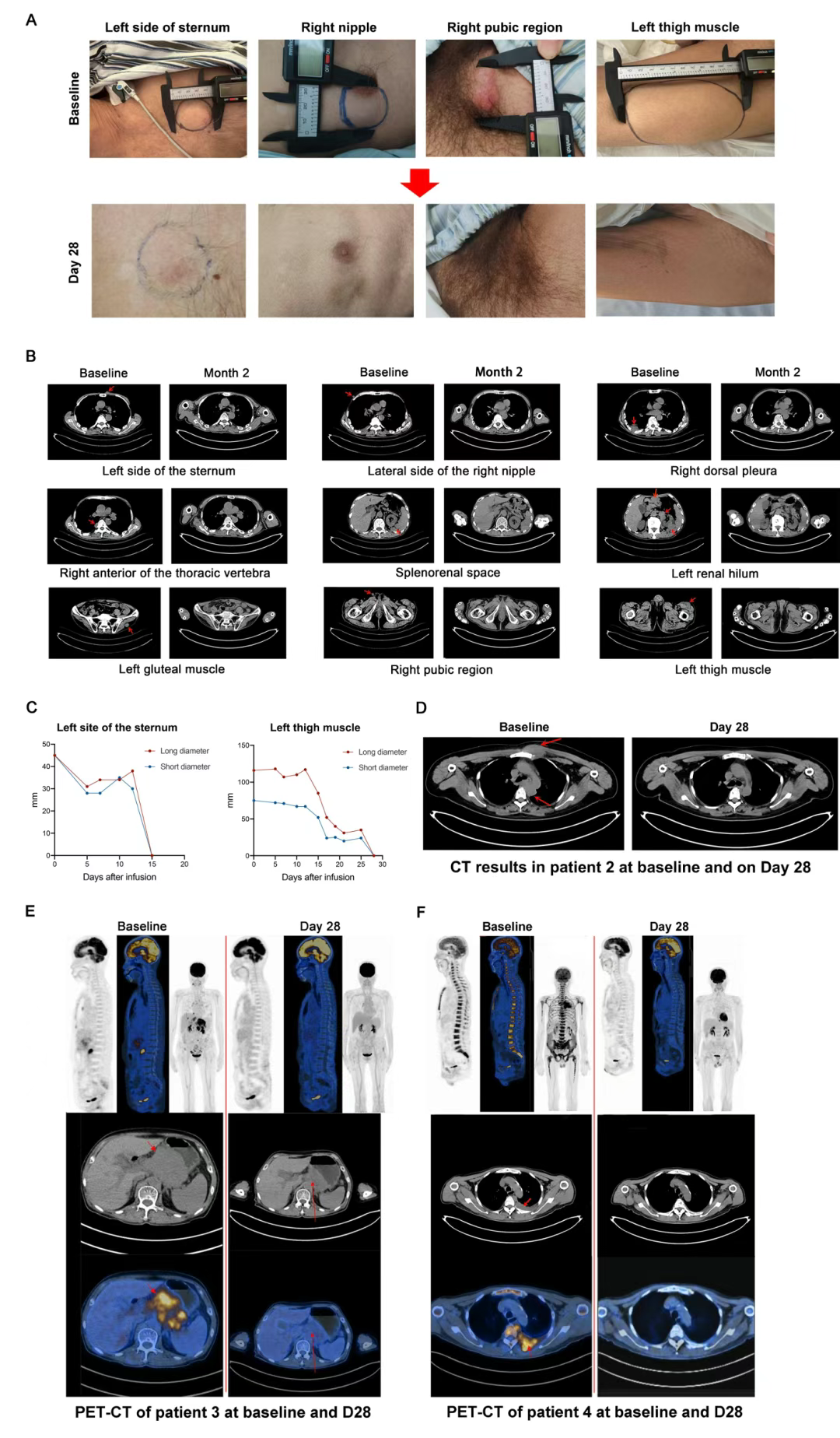
图4 (A)患者1肿瘤块的可见变化。(B)患者1在不同时间点的影像结果。(C)患者1肿瘤块的测量结果。(D)患者2、(E)患者3和(F)患者4在不同时间点的影像结果。
值得注意的是,ESO-T01是一种“现成的”单剂量治疗,直接全身给药,这些患者治疗前无需进行淋巴细胞清除(清淋),且ESO-T01对髓外病灶、脑脊液等传统CAR-T难以浸润的部位也表现出良好的疗效。
②试水自免潜力大
Capstan Therapeutics(现为艾伯维子公司)的核心平台技术涉及专有的tLNP递送载体,包括可I电离脂质(L829)、II靶向部分(如抗体)和III包裹的mRNA负载物。
L829脂质被设计用于减少肝脏摄取,提高向免疫细胞的mRNA递送效率。通过将抗CD5或抗CD8抗体偶联到L829-tLNP上,实现了对T细胞的特异性靶向,递送RNA有效载荷,包括mRNA或基因编辑工具,能够在体内重新编程特定细胞类型。
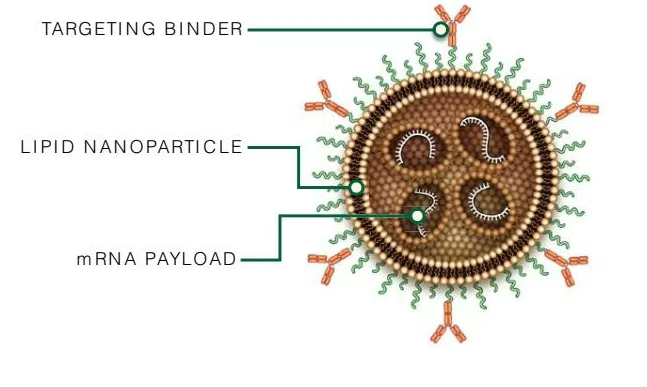
图5靶向脂质纳米颗粒(tLNP)的示意图。
6月,Capstan公司在Science上发表的tLNPs临床前研究数据显示,CD8-L829-tLNP-CD20能在非人灵长类动物中深度清除B细胞并实现“免疫重置”。
Capstan的主要体内CAR-T候选产品CPTX2309(CD8-L829-tLNP-CD19),由偶联到LNP表面的CD8靶向抗体组成,封装编码CAR的mRNA,该CAR与CD19(一种在B细胞上表达的细胞表面受体)结合。Capstan宣布CPTX2309于今年6月进入I期临床阶段,用于治疗B细胞介导的自身免疫性疾病。
02看看谁稳?商业化挑战的现实考量
两条技术路线都面临着各自的商业化挑战,这些挑战决定了它们能否从实验室成功走向市场。
2.1Allo CAR-T的挑战:安全性、生产复杂性与竞争
①安全性问题——警钟再次敲响
Allo CAR-T仍需面对宿主免疫排斥(移植物抗宿主病GvHD和宿主抗移植物反应HvG)的风险。尽管基因编辑技术降低了风险,但并未完全消除。
然而,更大的挑战可能来自为CAR-T细胞“腾地方”的淋巴细胞清除(Lymphodepletion)方案。
2025年8月,Allogene Therapeutics宣布,其II期ALPHA3研究中出现一例患者死亡案例。
调查结论指出,死亡与其同种异体CAR-T产品cema-cel本身无关,而是由清淋方案中的免疫抑制抗体ALLO-647引起。该患者在输注后第54天,因在免疫抑制状态下发生播散性腺病毒感染,最终导致肝功能衰竭。
此事件导致Allogene全面停止涉及ALLO-647的研究臂,并与FDA协商后,决定停止使用ALLO-647,将清淋方案换回标准的环磷酰胺+氟达拉滨(FC)方案。
②生产复杂性
虽然相对于自体CAR-T有所简化,但Allo CAR-T仍涉及供体细胞来源、复杂的体外基因编辑、扩增和质控流程。建立稳定、规模化且符合药品生产质量管理规范(GMP)的生产工艺是一项巨大挑战。
③激烈的市场竞争
血液肿瘤领域已有多个成熟的自体CAR-T产品上市,同时双特异性抗体、ADC药物等也在不断挤压市场空间。Allo CAR-T需在疗效、安全性或成本上展现出显著优势才能脱颖而出。
2.2 In Vivo CAR-T的挑战:技术成熟度、安全性与生产
①技术新颖,成熟度低
In Vivo CAR-T是一项更前沿的技术,其递送系统的效率、靶向性和安全性仍需大量临床数据验证。如何确保CAR基因在体内高效、精准地转导目标T细胞,同时避免脱靶效应,是技术成功的关键。
②独特的安全性担忧
I细胞因子释放综合征(CRS):尽管无需清淋,但In Vivo CAR-T在临床中已观察到较高级别(如3级)的CRS,需密切监测和管理。
ESO-T01的试验中,所有患者均出现了CRS(3例3级,1例1级),但未发生4级及以上的严重非血液学毒性,且所有不良事件均通过常规治疗(如糖皮质激素)得到控制。这表明In Vivo CAR-T的毒性目前看来是可控的,但CRS发生率似乎较高。
II递送系统本身的安全性:病毒载体可能存在免疫原性或基因组整合的潜在风险(虽经改造已降低),LNP递送mRNA也可能引起先天免疫反应。对体内基因修饰产品的长期安全性追踪至关重要。
③规模化生产与监管路径
病毒载体或LNP的生产本身具有挑战性,如何实现其稳定、大规模、合规的生产是产业化的前提。作为一种全新的治疗模式,监管机构如何审评批准这类“体内细胞疗法”也是一个需要探索的领域。
03未来展望:并行、互补与融合
生物医药技术的发展极少情况是“赢家通吃”。Allo CAR-T 和 In Vivo CAR-T 更可能的结局是在不同阶段和不同应用场景中找到各自的位置,甚至出现技术上的融合。
3.1短期并存与场景分化
Allo CAR-T可能凭借其相对更成熟的路径,在血液肿瘤领域率先实现更广泛的应用,特别是作为“现货型”产品解决自体CAR-T等待时间长的问题。
In Vivo CAR-T则因其潜在更好的安全性和便捷性,可能在自身免疫性疾病领域开辟出新天地,其“免疫重置”的潜力令人期待。
3.2长期可能的技术融合
未来的细胞治疗也许不会是单一的路线。例如,科学家们可能会探索利用基因编辑技术改造出“通用型”的底盘细胞,再通过体内递送系统进行二次精准调控或重编程,从而实现“1+1>2”的疗效,并进一步简化流程。
无论哪条路线更快取得成功,它们都在共同推动一个宏伟目标的实现:让更多患者能够用得上、用得起这些革命性的细胞疗法,最终重塑癌症和自身免疫性疾病的治疗格局。
参考资料:
1.https://allogene.com/
2.In-vivo B-cell maturation antigen CAR T-cell therapy for relapsed or refractory multiple myeloma. Xu, Jia et al. The Lancet, Volume 406, Issue 10500, 228 - 231.
3.https://www.esobiotec.com/
4.https://www.capstantx.com/
5.Hunter, Theresa L et al. “In vivo CAR T cell generation to treat cancer and autoimmune disease.” Science (New York, N.Y.) vol. 388,6753 (2025): 1311-1317. doi:10.1126/science.ads8473
6.FREDERICK L LOCKE. Allogeneic Chimeric Antigen Receptor T-Cell Products Cemacabtagene Ansegedleucel/ALLO-501 in Relapsed/Refractory Large B-Cell Lymphoma: Phase I Experience From the ALPHA2/ALPHA Clinical Studies.[J]. Journal of Clinical Oncology, 2025: 1695-1705. DOI:10.1200/JCO-24-01933.
7.Samer Ali Srour et al. ALLO-316 in advanced clear cell renal cell carcinoma (ccRCC): Updated results from the phase 1 TRAVERSE study.. JCO 43, 4508-4508(2025).DOI:10.1200/JCO.2025.43.16_suppl.4508
文章来源:小药说药
原文链接: https://mp.weixin.qq.com/s/WRnw59T3EVWcF6273yqdwQ












































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论