从这两款二代产品研发情况就可以看出,静脉铁研发难度不低。
二代未成,三代已至
二代静脉铁剂还未仿制成功,三代就已重磅来袭。
对于一次性需要输注大剂量铁剂的患者,二代静脉铁每次输注的剂量小,需多次输注,三代静脉铁可实现短时间内给予大剂量治疗。
2021年后,第三代静脉铁异麦芽糖酐铁和羧基麦芽糖铁在国内上市,三代上市后,销售额迅速增长,有取代二代静脉铁的趋势。
仁合益康被驳回的品种就是三代静脉铁,羧基麦芽糖铁注射液,原研Vifor,2022年11月进口中国上市,2024年就涨到了近4千万,对一个适应症较窄的品类来说,这样的增长速度已经算惊人了。
羧基麦芽糖铁,参比在2020年就已确立,2023年先声药业冲击该药品首仿,以失败告终,这两家企业均在首轮审评结束后收到不批准通知。当前,仅有四川汇宇进入补充资料审评阶段,有望成为该品种首仿的最终胜利者。
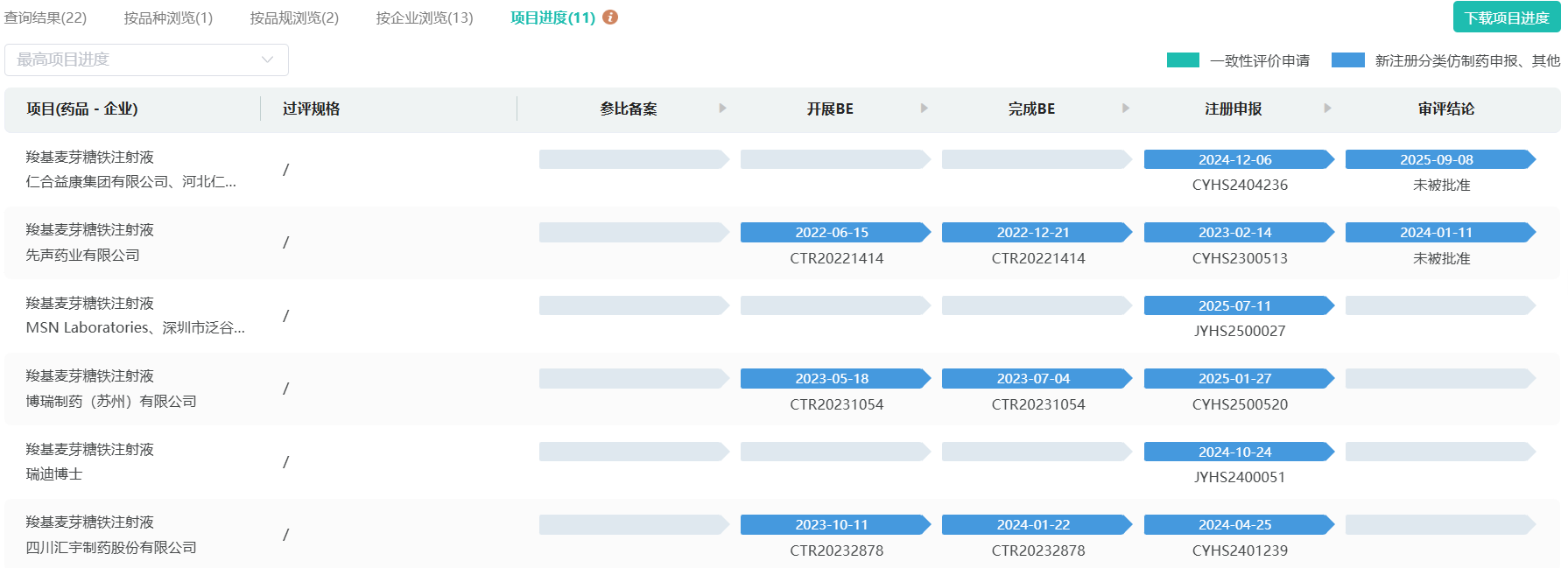
截图来源:摩熵医药数据库
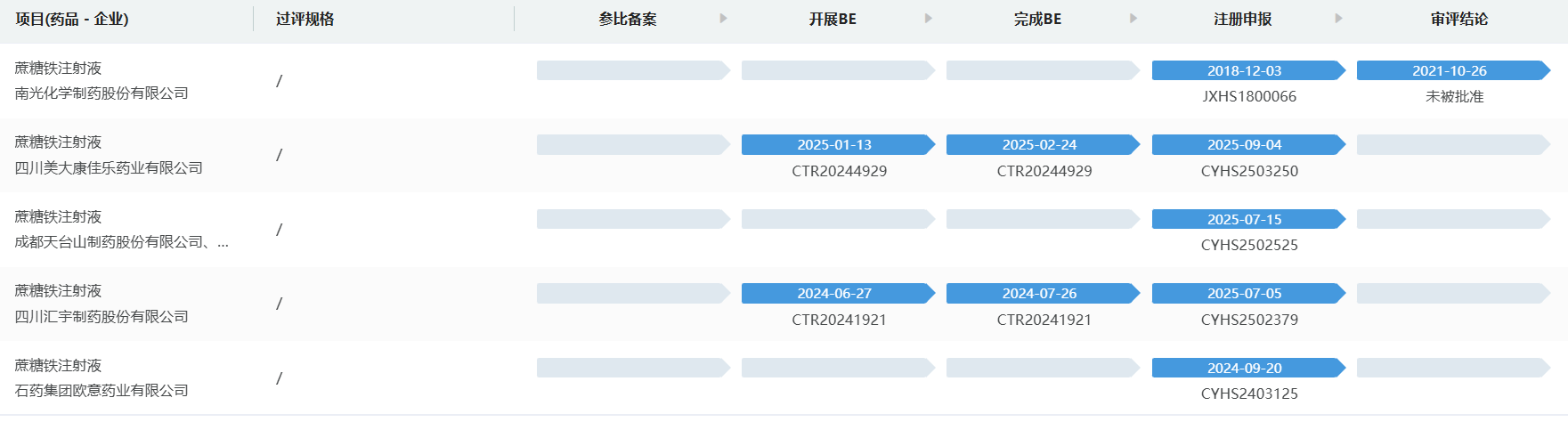
异麦芽糖酐铁,原研Pharmacosmos,2021年1月进口中国上市,无国内仿制上市,市场增速同样惊人,三年到达3千万以上,参比于2022年确立,暂无厂家报产,仁合益康和正大天晴正在进行BE试验。
仿制这么难?
从被驳回的羧基麦芽糖铁注射液进行简单分析。
羧基麦芽糖铁并非传统小分子药物,而是一种典型的非生物复杂药物,特点在于结构不可完全表征和工艺决定产品,这意味着,简单的化学成分复制(Q1/Q2一致)是远远不够的。
羧基麦芽糖铁从原料药到制剂工艺难度都很高:原料制备需要将三价铁离子与特定分子量的羧基化多糖配体络合,形成结构稳定的纳米胶体。此过程涉及多个关键步骤,每一步都必须精确控制,以确保最终产物的关键质量属性与原研药一致。
制剂工艺相对简单,主要是将API溶解于注射用水中,调节pH值和渗透压,然后进行除菌过滤和无菌灌装,尽管处方简单,但工艺控制依然是关键。
再者羧基麦芽糖铁证明BE等效难度同样不低,FDA发布过羧基麦芽糖铁的BE指南,依据FDA发布的指导原则,体外BE研究是强制性的,其核心是证明仿制药与原研药在粒径分布上的等效性。
FDA为体内BE研究提供了两种战略路径,方案一(患者)、方案二(健康人)、需要在风险、成本和时间之间进行权衡。
羧基麦芽糖铁注射液仿制从原料到制剂再到BE试验都要求极高,稍微出错就将前功尽弃,难度确实大。
希望汇宇能成功首仿。
参考来源
[1] 摩熵医药(原药融云)数据库
[2] 最新!羧基麦芽糖铁注射液首仿被拒
[3] 羧基麦芽糖铁注射液—阳村指南
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论